L'évaporation se produit lorsqu'un liquide se transforme en gaz. Avez-vous déjà remarqué que lorsqu’un verre est laissé sur le comptoir, l’eau commence à s’évaporer ? C’est de l’évaporation, pas des fées assoiffées qui habitent dans votre cuisine. L'évaporation est le processus par lequel les molécules subissent une transition spontanée de la phase liquide à la phase gazeuse. L'évaporation est l'opposé de la condensation.
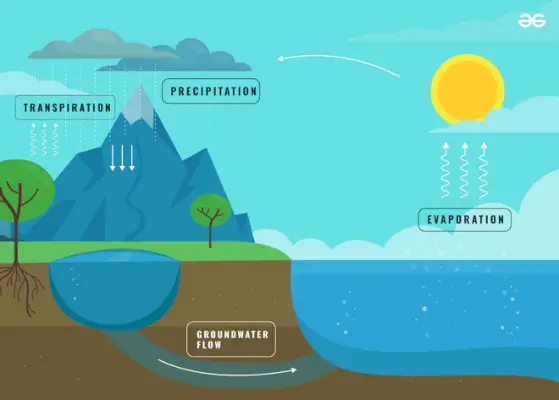
Évaporation
Un type de vaporisation appelé évaporation implique le transfert de particules liquides dans la phase gazeuse et a généralement lieu à la surface des liquides. En conséquence, il est affirmé que ce processus implique un changement dans l’état de la matière des liquides.
Table des matières
contacts bloqués
- Qu’est-ce que l’évaporation ?
- Exemples d'évaporation
- Processus d'évaporation
- Facteur affectant l'évaporation
- Différence entre l'évaporation et l'ébullition
- Différence entre évaporation et vaporisation
Qu’est-ce que l’évaporation ?
L'évaporation est un processus par lequel l'état liquide de la matière est converti en un état gazeux en présence de chaleur.
Beaucoup de gens confondent évaporation et ébullition, car lors de l’ébullition, le liquide passe également à l’état gazeux. Mais il y a une différence. La toute première est que l’ébullition du liquide se produit à une température particulière, tandis que l’évaporation peut se produire à n’importe quelle température inférieure au point d’ébullition. De plus, l’ébullition est un phénomène global, tandis que l’évaporation est un phénomène de surface, ce qui signifie que l’évaporation ne peut se produire qu’à la surface du liquide.

Lors de l'évaporation, la molécule ayant une énergie cinétique plus élevée ne se dissipe que de la couche supérieure du liquide. Il existe également une propriété unique de l’évaporation qui provoque un effet de refroidissement. Le pot en terre était utilisé pour stocker de l'eau fraîche en été, car l'eau s'écoulait des minuscules pores du pot, provoquant une évaporation et conduisant au refroidissement de l'eau à l'intérieur du pot. Desert Cooler fonctionne également sur le principe de l’évaporation.
Pour que l’évaporation se produise, les molécules d’un liquide doivent être proches de la surface, doivent s’éloigner du corps du liquide et doivent avoir suffisamment d’énergie cinétique pour s’échapper de l’interface. Lorsque des molécules s’échappent, l’énergie cinétique moyenne des molécules restantes diminue. Cela abaisse la température du liquide et constitue la base du phénomène de refroidissement par évaporation.
L'évaporation dépend également de certains facteurs, comme la température, la surface du liquide, la vitesse du vent et l'humidité. Nous en discuterons en détail dans cet article.
Exemples d'évaporation
Il existe de nombreux exemples d’évaporation mais nous n’en abordons ici que quelques-uns :
- Séchage des vêtements au soleil : Nous avons tous séché nos vêtements au soleil, les vêtements mouillés sèchent à cause de l'évaporation où l'eau se transforme en vapeur d'eau.
- Assèchement des plans d’eau : Nous avons constaté en été que l'eau des étangs et des lacs diminuait ou parfois s'asséchait à cause de l'évaporation.
- Cycle de l'eau: C'est un très bon exemple d'évaporation. Dans les deux cas ci-dessus, nous avons expliqué comment l'évaporation transforme l'eau en vapeur d'eau. Cette vapeur d’eau monte ensuite vers le ciel et se condense pour former un nuage, qui ensuite se précipite. L’évaporation est donc importante pour réguler le cycle de l’eau.
- Formation de sel : Naturellement ou industriellement, le sel se forme en raison de l'évaporation où l'eau s'évapore pour nous laisser du sel.
- Séchage d'un sol lavé
- Travailler dans la glacière du désert en été.
Processus d'évaporation
Un liquide s'évapore lorsqu'il est chauffé. Cela implique que les molécules du liquide doivent acquérir de l’énergie cinétique. Les molécules d’un liquide se dilatent et vibrent plus rapidement à mesure qu’elles acquièrent de l’énergie cinétique. Le liquide se transforme alors en gaz, modifiant ainsi son état de la matière.
L'eau est une substance courante où se produit l'évaporation. L'eau passe d'un liquide à un gaz lorsqu'on lui applique de l'énergie ou de la chaleur, car les liaisons qui maintiennent les molécules ensemble commencent à s'affaiblir. Le point d’ébullition de l’eau, qui est de 212 degrés Fahrenheit ou 100 degrés Celsius, est le point auquel elle se transforme d’un liquide en gaz.
Facteur affectant l'évaporation
L’évaporation facilite notre vie à bien des égards, et même elle contribue également au cycle de l’eau. Mais l’évaporation dépend de certains facteurs qui vont contrôler le taux d’évaporation. Une autre chose à noter est que l’évaporation est un processus lent, mais certains facteurs externes augmentent ou ralentissent le taux d’évaporation. Discutons de tous ces facteurs d’évaporation :
Température
Le tout premier facteur est la température puisque nous savons que l’évaporation peut se produire à n’importe quelle température avant le point d’ébullition, mais la température joue également un rôle dans l’évaporation. Cela déterminera le taux d’évaporation, plus la température est élevée, plus le taux d’évaporation est élevé. Maintenant la question est comment ? Nous savons tous que la température augmentera l’énergie cinétique, car c’est l’énergie utilisée pour briser les forces intermoléculaires qui lient la molécule liquide. Ainsi, lorsque nous appliquons plus de températures, la molécule brise rapidement ses forces intermoléculaires et s’évapore.
Cela implique,
Température ∝ Évaporation
Par exemple, nous avons tous vu dans la chaleur de l'été, les vêtements sèchent plus rapidement que les jours normaux. Cela est dû au facteur Température.
Doit vérifier
- Unité de température
- Relation entre les échelles de température Celsius et Kelvin
- Effet du changement de température
Surface du liquide
Plus tôt, nous avons expliqué que l’évaporation est un phénomène de surface et que la surface joue un rôle dans le taux d’évaporation. Plus la surface est grande, plus le taux d'évaporation sera élevé. Ainsi, s’il y a plus de surface, plus de molécules liquides seront présentes à la surface, ce qui signifie que davantage de molécules rompront leurs liaisons intermoléculaires, ce qui augmentera le taux d’évaporation. Nous pouvons donc l'écrire ainsi :
Surface du liquide ∝ Évaporation
Par exemple, la même quantité d’eau s’évapore plus rapidement dans une assiette que l’eau dans une tasse peu profonde, car l’assiette offre une plus grande surface pour le liquide que la tasse peu profonde.
Humidité
L'humidité fait référence à la quantité d'humidité ou vapeur d'eau dans l'air . Plus il y a de vapeur d’eau dans l’air on dira plus d’humidité. Avec plus d’humidité, le taux d’évaporation diminue.
Humidité ∝ 1/Évaporation
Par exemple, pendant la saison des pluies, lorsque notre environnement est plus humide, il est très difficile de sécher nos vêtements.
Vitesse du vent
La vitesse du vent est directement proportionnelle à l’évaporation, ce qui signifie qu’avec l’augmentation de la vitesse du vent, le taux d’évaporation augmenterait.
quelle est la taille de mon écran d'ordinateur
Vitesse du vent ∝ Évaporation
Par exemple, lors d’une journée venteuse, les vêtements sèchent plus rapidement que les jours normaux. En effet, le vent a réduit l'humidité, ce qui augmentera le taux d'évaporation.
Lire aussi
- Effets de l'humidité relative et de la vitesse du vent
Différence entre l'évaporation et l'ébullition
Vous trouverez ci-dessous les principales différences entre l’évaporation et l’ébullition.
| Évaporation | Ébullition |
|---|---|
| L'évaporation est un processus naturel dans lequel le liquide se transforme en forme gazeuse en raison d'une augmentation de la température, de la pression, ou des deux. | L'ébullition est simplement la vaporisation, qui transforme le liquide en gaz par chauffage continu. |
| L'évaporation se produit uniquement à la surface du liquide. | Cependant, l'ébullition se produit dans toute la grande masse de la substance. |
| En cas d'évaporation, la température ne dépasse pas le point d'ébullition du liquide. | Cependant, lors de l’ébullition, le processus ne se produit qu’au point d’ébullition du liquide. |
| Il s’agit donc d’un processus lent. | Il s’agit donc d’un processus rapide. |
| Le taux d’évaporation augmente avec l’augmentation de la surface ouverte du liquide. | La vitesse d’ébullition est indépendante de la surface ouverte du liquide. |
Différence entre évaporation et vaporisation
La différence entre évaporation et vaporisation est indiquée ci-dessous :
| Évaporation | Vaporisation |
|---|---|
| Phénomène de surface | Phénomène de masse |
| Se produit à n’importe quelle température | Se produit à une température spécifique |
| Se produit uniquement à la surface d'un liquide | Se produit dans la majeure partie du liquide |
| Le processus est plus lent | Le processus est relativement plus rapide |
| Pas facilement visible | Visible pendant l'ébullition |
| La chaleur requise pour l’évaporation est moindre | La chaleur requise pour la vaporisation est plus |
| Exemples : séchage de vêtements, flaques d'eau | Exemples : eau bouillante, formation de vapeur |
Doit lire
- L'évaporation provoque un refroidissement
- Séparation par évaporation
- Cristallisation
Évaporation – FAQ
Quelle est la différence entre évaporation et vaporisation ?
Le changement de phase d'une substance ou d'un élément qui a lieu pendant le processus d'ébullition ou de sublimation est appelé vaporisation. En termes simples, l’évaporation est une forme de vaporisation qui se produit principalement lorsque la température est inférieure au point d’ébullition. L’état d’une substance peut passer d’un solide ou d’un liquide à un gaz par vaporisation.
Quels sont les facteurs affectant l’évaporation ?
Voici quelques facteurs qui déterminent le taux d’évaporation :
- Surface du liquide : Plus la surface est grande, plus le taux d’évaporation sera élevé. Ainsi, la Surface du liquide ∝ Évaporation.
- Humidité : Avec plus d'humidité, le taux d'évaporation diminue, ce qui signifie Humidité ∝ 1/Évaporation.
- Vitesse du vent : la vitesse du vent est directement proportionnelle à l'évaporation, ce qui signifie qu'avec l'augmentation de la vitesse du vent, il y aurait une augmentation du taux d'évaporation.
En quoi l’évaporation diffère-t-elle de l’ébullition ?
Le processus d’évaporation est très différent de l’ébullition à bien des égards. L'évaporation est un processus naturel dans lequel le liquide se transforme en forme gazeuse en raison d'une augmentation de la température, de la pression, ou des deux. Cependant, l’ébullition n’est pas un processus naturel, c’est simplement la vaporisation, qui transforme le liquide en gaz par chauffage continu.
Comment se produit l’évaporation dans le cycle de l’eau ?
Lorsque la lumière du soleil réchauffe la surface de l’eau, l’évaporation se produit dans le cadre de la cycle de l'eau . La chaleur du soleil fait voyager les molécules d’eau de plus en plus vite jusqu’à ce qu’elles puissent s’échapper sous forme de gaz. Une molécule de vapeur d’eau passe environ 10 jours dans l’atmosphère après s’être évaporée.
comment déréférencer un pointeur en c
Qu’est-ce que l’évaporation ? Donne un exemple.
L'évaporation est un processus par lequel l'état liquide de la matière se transforme en un état gazeux en présence de chaleur. Par exemple, nous avons tous séché nos vêtements au soleil, les vêtements mouillés sèchent à cause de l'évaporation où l'eau se transforme en vapeur d'eau.
Pourquoi est-il très difficile de sécher les vêtements pendant la saison humide ?
Puisque nous savons que l’humidité fait référence à la quantité d’humidité ou de vapeur d’eau dans l’air. Plus il y a de vapeur d’eau dans l’air, dirons-nous, plus il y a d’humidité. Avec plus d'humidité, le taux d'évaporation diminue. Ainsi, il deviendra très difficile de sécher les vêtements pendant la saison humide.
Écrivez quatre exemples d’évaporation.
Des exemples d'évaporation sont les suivants :
- Assèchement des plans d'eau
- Cycle de l'eau
- Formation de sel
- Séchage d'un sol lavé
Comment l’augmentation de la température affecte-t-elle le taux d’évaporation ?
Plus la température est élevée, plus le taux d'évaporation est élevé. En effet, la température augmentera l’énergie cinétique et l’énergie utilisée pour briser les forces intermoléculaires qui lient la molécule liquide. Ainsi, lorsque nous appliquons plus de température, la molécule brise rapidement ses forces intermoléculaires et s’évapore.
Quel est l’opposé de l’évaporation ?
Condensation est l’opposé de l’évaporation. Un type de vaporisation appelé évaporation implique le transfert de particules liquides dans la phase gazeuse et a généralement lieu à la surface des liquides. En conséquence, il est affirmé que ce processus implique un changement dans l’état de la matière des liquides.
