Densité de l'eau est le rapport entre la masse et le volume de l'eau à température ambiante est de 998,2 kg/m3. La densité de toute substance est définie comme la quantité de masse présente dans l’unité de volume de la substance donnée.
Pour l'eau pure, la densité est 1 g/cm 3 ou 1000kg/m 3 . La densité de l'eau pure varie avec la température et atteint son point culminant à une température de 4 °C, soit 1 000 kg/m.3.
La densité de l'eau est maximale à 4 °C.
Quelle est la densité de l’eau ?
Le terme densité fait référence au volume (espace) occupé par un objet ou une substance par rapport à la quantité de matière qu'il contient (sa masse). Une autre façon de considérer la densité est la quantité de masse par unité de volume. Un objet à haute densité est solide et compact. L'unité SI de densité est kg/m3et g/cm3dans le système CGS. C'est une propriété intrinsèque de la matière.
La densité de l'eau est de 1 g/cm3ce qui n'est pas une coïncidence. La densité est le rapport entre la masse de la matière et le volume qu'elle occupe, utilisé pour calculer la densité de 1 g d'eau qui occupe 1 cm.3volume. De plus, la pression atmosphérique et la température atmosphérique affectent également la densité réelle de l’eau.
tri par fusion en Java
Cependant, ces différences de densité sont relativement faibles, vous pouvez donc continuer à utiliser 1 g/cm3pour la densité de l'eau, sauf si vous devez effectuer des calculs très spécifiques ou si l'expérience est menée dans des conditions de températures ou de pressions extrêmes.
Cependant, la densité de l'eau pour différents systèmes métriques est donnée ci-dessous :
| Densité de l'eau | Système d'unité | Densité de l'eau |
| Densité de l'eau en g/cm3 | 1 g/cm3 | |
| Densité de l'eau en g/mL | 1 g/ml | |
| Densité de l'eau en kg/m3 | 1000kg/m3 | |
| Densité de l'eau en lb/pi3 | 62,4 lb/pi3 |
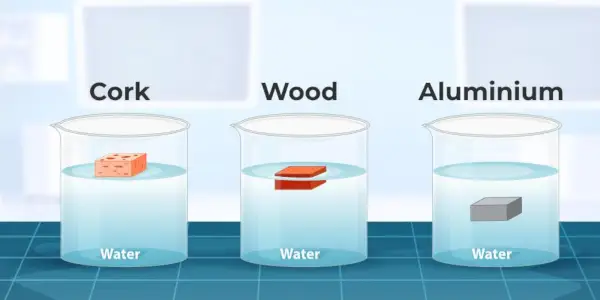
La substance dont la densité est inférieure à celle de l'eau flotte sur l'eau et la substance dont la densité est supérieure à l'eau coule dans l'eau.
L'image ci-dessous montre trois conteneurs dans le premier conteneur, la densité du liège est inférieure à celle de l'eau donc il flotte sur l'eau, dans le deuxième conteneur la densité du bois est presque égale à celle de l'eau donc il est partiellement immergé dans l'eau, et dans le troisième récipient, la densité du liège et de l'aluminium est supérieure à celle de l'eau donc il coule dans l'eau.
Gardez à l’esprit que ces chiffres de densité de l’eau s’appliquent uniquement à l’eau pure. La densité de l'eau salée (comme celle des océans) varie en fonction de la quantité de sel dissoute dans l'eau. La densité de l'eau de mer est normalement comprise entre 1,02 g/cm3et 1,03 g/cm3, ce qui est légèrement supérieur à la densité de l'eau pure.
Propriétés de l'eau
L’eau est un liquide étrange, c’est le liquide le plus important pour la survie des humains. Diverses propriétés de l'eau sont discutées ci-dessous,
| Densité de l'eau | 997 kg/m³ |
|---|---|
| Formule d'eau | H2Ô |
| Masse molaire de l'eau | 18,015 g/mole |
| Point d'ébullition de l'eau | 100 °C |
| Point de fusion de l'eau | 0 °C |
Densité de la formule de l'eau
La densité de l'eau est calculée à l'aide de la formule de densité normale,
D = M/V
où,
D est la densité de l'eau
M est la masse de l'eau
DANS est le volume de l'eau
Nous savons que,
À température ambiante, si le volume d’eau est de 1 ml, sa masse est de 0,995 gramme. Maintenant, la densité de l'eau est,
D = masse/volume
= 0,995/1
= 0,995 g/ml = 0,995 g/cm3
En savoir plus sur Densité et Structure et propriétés de l'eau
Comment calculer la densité de l'eau ?
Un cylindre gradué est utilisé pour calculer la densité de l’eau. Un cylindre vide est prélevé et pesé sur une machine. Cela nous donne la masse d’un cylindre gradué vide, soit m.
Maintenant, la quantité d'eau requise est versée dans le cylindre et elle est à nouveau pesée. Cela nous donne la masse de l’éprouvette graduée remplie, soit m’.
Maintenant, la différence entre les masses calculées nous donnerait la masse d’eau. Ainsi,
Masse d'eau (M) = m' – m
Le volume d'eau (V) se trouve en utilisant le marquage sur le cylindre. On constate que le volume de l’eau est presque égal à sa masse.
Donc, en utilisant la formule de densité que nous obtenons,
ρ = Masse d'eau/Volume d'eau
ρ = M/V [car la masse (M) et le volume (V) sont presque égaux]
ρ = 1 g/ml
On conclut que la densité de l’eau est une valeur constante, c’est-à-dire 1g/ml ou 1 g/cm 3 .
Densité de l'eau à température ambiante
À température ambiante, c'est-à-dire à une température de 20 °C à 25 °C, la densité de l'eau est de 0,9982 g/cc, soit 998,2 kg/m.3. La masse d’eau est presque égale à son volume à température ambiante et l’eau reste sous forme liquide à température ambiante. L'eau de mer contient divers sels et minéraux dissous, sa densité est donc légèrement supérieure à celle de l'eau normale. Normalement, la densité de l'eau de mer est d'environ 1027 kg/m3.
Facteurs affectant la densité de l'eau
Un certain nombre de facteurs peuvent affecter la densité d’une substance. Certains des facteurs qui affectent la densité de l’eau sont répertoriés ci-dessous :
La densité de l'eau est d'environ 1 gramme par centimètre cube (1 g/cm3).
- Bien que la relation soit décrite comme non linéaire et unimodale plutôt que monotone, elle dépend de la température.
- L'eau liquide a tendance à devenir plus dense lorsqu'elle est refroidie par rapport à la température ambiante, mais on pense que l'eau pure atteint sa densité maximale à environ 4 °C et que de 4 °C à 0 °C, la densité de l'eau augmente, et ce comportement est appelé comportement anormal. comportement de l'eau.
- À mesure qu’il refroidit, il a tendance à se dilater et à devenir moins dense. Ainsi, l'eau est un liquide étrange qui devient plus dense jusqu'à un point spécifique lors du refroidissement, puis commence à se dilater lors d'un refroidissement ultérieur.
Densité de l'eau à différentes échelles de température
Le tableau suivant montre la densité de l'eau (en g/cm3) à différentes valeurs de températures (en °C)
| Température (en C) | Densité de l'eau (gm/cm3) |
|---|---|
| -30° | 0,98385 |
| -20° | 0,99355 |
| -10° | 0,99817 |
| 0° | 0,99987 |
| 4,0° | 1.00000 |
| 10ème | 0,99975 |
| 21° | 0,99802 |
| 48,9° | 0,98870 |
| 60° | 0,98338 |
| 71,1° | 0,97729 |
| 82,2° | 0,97056 |
| 93,3° | 0,96333 |
| 100° | 0,95865 |
Comme on l'observe, l'eau a une densité exactement égale à 1 g/cm.3seulement à 4 °C. De plus, il a été observé que la densité de l’eau diminue avec l’augmentation de la température. La glace a une densité inférieure à celle de l’eau, ce qui entraîne une baisse de la densité de l’eau. C’est la raison pour laquelle la glace flotte au-dessus de l’eau et pourquoi les glaçons ne tombent pas simplement au fond d’un verre d’eau lorsque vous les y mettez.
Expansion anormale de l'eau
L'eau se comporte anormalement lors du chauffage, c'est-à-dire que sa dilatation n'est pas linéaire. Sa densité a d’abord augmenté de 0 °C à 4 °C, puis elle a commencé à diminuer à mesure que son volume commençait à augmenter.
Il est désormais évident que sa densité est maximale à 4 °C
La densité maximale de l'eau est à 4°C soit 1g/cm3ou 1000 kg/m3.
Densité vs température
Puisque sa densité change avec la température, l’eau n’a pas de densité absolue. La forme liquide a une densité plus élevée que la forme solide. Pour savoir comment la densité varie en fonction de la température, regardez le graphique de densité en fonction de la température ci-dessous.
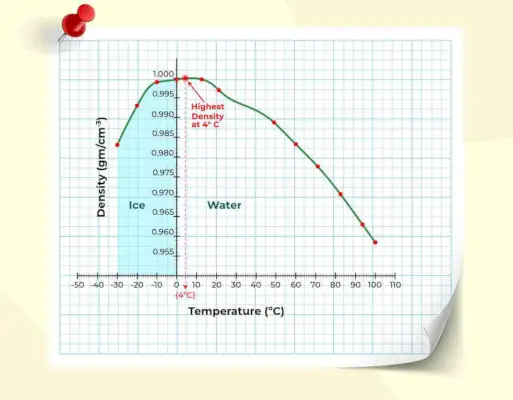
Densité de l'eau maximale à 4 °C ?
L'eau est un liquide étrange et se comporte anormalement. La densité de l’eau est maximale à 4 °C et cela peut s’expliquer ainsi :
- Lorsque l'eau gèle, ses particules se rapprochent jusqu'à atteindre leur densité maximale à 4°C. À cette température, l'eau est uniquement à l'état liquide.
- Après une nouvelle diminution de la température, l'eau a tendance à geler et à acquérir un état solide.
- On pourrait penser que l'eau solide serait plus dense, mais à mesure que l'eau commence à geler, elle acquiert une structure en forme de cage qui finit par augmenter le volume de l'eau et c'est la raison pour laquelle la glace flotte sur l'eau.
- Maintenant, comme nous le savons, si le volume augmente, la densité diminue. Ainsi, la densité de l’eau diminue après 4°C.
Il est donc clair que la densité de l'eau est maximale à 4°C
Vérifier: Formule de pression d'eau
Expérience sur la densité de l'eau
Afin de mieux comprendre la densité de l’eau, son comportement et sa comparaison avec d’autres substances. Réalisons l’activité mentionnée ci-dessous :
Prenez une petite quantité de liquides visqueux comme de l'eau, par ex. Savon liquide, lait, sirop de sucre, miel, alcool éthylique et huile d'olive dans un tube à essai. Mélangez-les bien afin que chacune des substances ne puisse pas être clairement observée.
Maintenant, laissez-le pendant quelques heures pour que la couche de chaque substance se stabilise à un certain niveau, comme indiqué ci-dessous :

Or, il a été observé que différentes substances ont une densité différente. Cela implique que chaque substance pèse différemment pour le même volume. Parce que leur poids varie, les substances plus lourdes ont tendance à se déposer au fond, comme le miel, et le sirop de sucre et les matières plus légères comme l'huile d'olive et l'alcool éthylique ont tendance à flotter au sommet.
Densité des liquides courants
Différents liquides ont des densités différentes car ils ont des masses différentes pour un volume fixe de liquide. Le tableau ci-dessous nous indique la densité de divers liquides à température ambiante.
| Matériel | Densité (gramme/cm3) |
|---|---|
| Huile de lampe | 0,8 |
| Eau | 1.0 |
| Lait | 1.03 |
| Savon liquide | 1.06 |
| Chéri | 1,42 |
| glycérine | 1 260 |
| Mercure | 13h55 |
En savoir plus,
- La loi de Pascal
- Flottabilité
- Le principe de Bernoulli
Exemples résolus sur la densité de l'eau
Exemple 1 : Calculez la densité de l'eau si la masse de l'éprouvette graduée vide est de 10,2 g et celle de celle remplie est de 20 g.
Solution:
Nous avons,
m' = 20
m = 10,2
Calculez la masse d'eau.
M = m’ – m
M = 20 – 10,2
M = 9,8 g
Donc, volume (V) = 9,8 ml
En utilisant la formule que nous obtenons,
ρ = M/V
= 9,8/9,8
= 1g/ml
Exemple 2 : Calculez la masse de l'éprouvette graduée remplie si la masse d'eau est de 5 g et la masse de l'éprouvette vide est de 15 g.
Solution:
Nous avons,
M = 5
m = 15
En utilisant la formule que nous avons,
M = m’ – m
m' = M + m
m' = 5 + 15
m' = 20g
Ainsi, la masse requise de l’éprouvette graduée remplie est 20 g.
Vérifier: Différence entre la densité et la gravité spécifique
Densité de l'eau – FAQ
La densité de l'eau est maximale à quelle température ?
La densité de l'eau est maximale à 4°C ou à 39°F.
Quelle est la densité de l'eau ?
La densité d'une substance est définie comme la masse de cette substance répartie sur une unité de volume. Il est désigné par le symbole rho (ρ). Son unité de mesure standard est le kilogramme par mètre cube (kg/m3) et la formule dimensionnelle est donnée par [M1L-3T0].
Pourquoi la densité de l'eau est supérieure à celle de la glace ?
La densité de l'eau est supérieure à celle de la glace, car à mesure que l'eau forme de la glace, son volume augmente à mesure qu'elle forme une structure en forme de cage.
Pourquoi la glace flotte-t-elle dans l'eau ?
À environ 4° Celsius, l’eau a sa densité la plus élevée. La glace flotte car sa densité est inférieure à celle de l’eau liquide. Lors de la congélation, la densité de la glace diminue d'environ 9 %.
diviser une chaîne en C++
Comment la température affecte-t-elle la densité de l’eau ?
La densité de l'eau change avec la température. Elle augmente lorsque l'eau se refroidit jusqu'à 4°C et diminue lorsque la température descend au-dessus ou en dessous de ce point. Par exemple, à 100°C, la densité est d’environ 958,4 kg/m³, et à -30°C, elle est d’environ 983,854 kg/m³.
Pourquoi la densité de l’eau atteint-elle un maximum à 4°C ?
À environ 4°C, l’eau atteint sa densité maximale en raison d’un équilibre de forces moléculaires concurrentes. En dessous de cette température, l’eau commence à se dilater à mesure qu’elle se prépare à geler, c’est pourquoi la glace flotte sur l’eau liquide.
La présence de sels et de minéraux affecte-t-elle la densité de l’eau ?
Oui, la densité de l’eau peut augmenter avec la présence de sels dissous, de minéraux et d’autres substances. L'eau de mer, par exemple, est plus dense que l'eau douce, avec des densités typiques autour de 1 027 kg/m³ à la surface en raison de sa teneur en sel.
Quelle est la densité de l'eau de mer ?
La densité de l'eau de mer, en surface 1027 kg/m3environ.
Quelle est la densité de l’eau à température ambiante ?
La densité de l'eau à température ambiante est de 998,2 kg/m3.
